Hay parásitos que hacen ruido y parásitos que pasan casi desapercibidos hasta que el sistema de salud pública levanta una alerta. El Cryptosporidium pertenece a la segunda categoría. La mayoría de las personas lo desconoce por su nombre, pero este protozoo ha protagonizado algunos de los mayores brotes de diarrea transmitida por agua en la historia reciente, incluyendo uno en Milwaukee en 1993 que afectó a 403.000 personas en una sola ciudad.
Lo que hace especialmente difícil de controlar a este parásito es su resistencia al cloro: las concentraciones habituales de desinfectante en el agua corriente no eliminan sus ooquistes. Eso lo convierte en una amenaza real incluso en países con infraestructura de saneamiento avanzada. Y en personas con el sistema inmunitario comprometido, la infección puede pasar de molestia intestinal a problema grave sin tratamiento claramente efectivo.
Esta guía explica qué es la criptosporidiosis, cómo se transmite, qué síntomas produce y qué opciones existen tanto para el diagnóstico como para el manejo clínico. Para una visión general de las infecciones parasitarias intestinales, consulta también la guía sobre parásitos intestinales síntomas y tratamiento.
Lo esencial sobre la criptosporidiosis
Protozoo coccidio del género Cryptosporidium · Resistente al cloro a concentraciones estándar · Transmisión principalmente hídrica y fecal-oral · Síntoma principal: diarrea acuosa profusa · Diagnóstico: tinción ácido-alcohol resistente, PCR, ELISA · Tratamiento: nitazoxanida en inmunocompetentes · Sin cura establecida en inmunocomprometidos graves.
¿Qué es el Cryptosporidium?
Cryptosporidium parvum y hominis: las especies que afectan a humanos
El género Cryptosporidium incluye más de 40 especies reconocidas, pero dos concentran prácticamente todos los casos humanos: Cryptosporidium parvum y Cryptosporidium hominis. La diferencia entre ambas tiene implicaciones epidemiológicas claras.
C. parvum es una especie zoonótica: infecta tanto a humanos como a animales, especialmente a terneros y otros rumiantes jóvenes. Los trabajadores agrícolas y las personas que tienen contacto con ganado tienen un riesgo elevado por esta vía. C. hominis, en cambio, circula casi exclusivamente entre humanos. Ambas producen un cuadro clínico prácticamente idéntico, así que la distinción importa más para el epidemiólogo que para el paciente.
Este parásito pertenece al grupo de los coccidios, igual que Toxoplasma gondii o Cyclospora, y aunque se clasifica como protozoo, tiene características moleculares que lo acercan a los hongos, lo que explica en parte por qué los antiparasitarios convencionales no funcionan bien contra él.
El ciclo de vida y el papel de los ooquistes
El ooquiste es la forma infectante y la clave de todo el problema. Estos ooquistes son estructuras de paredes gruesas, de apenas 4-6 micrómetros de diámetro, que el parásito produce en el intestino del huésped y que salen con las heces en cantidades enormes — hasta 109 ooquistes por gramo de heces durante la fase aguda.
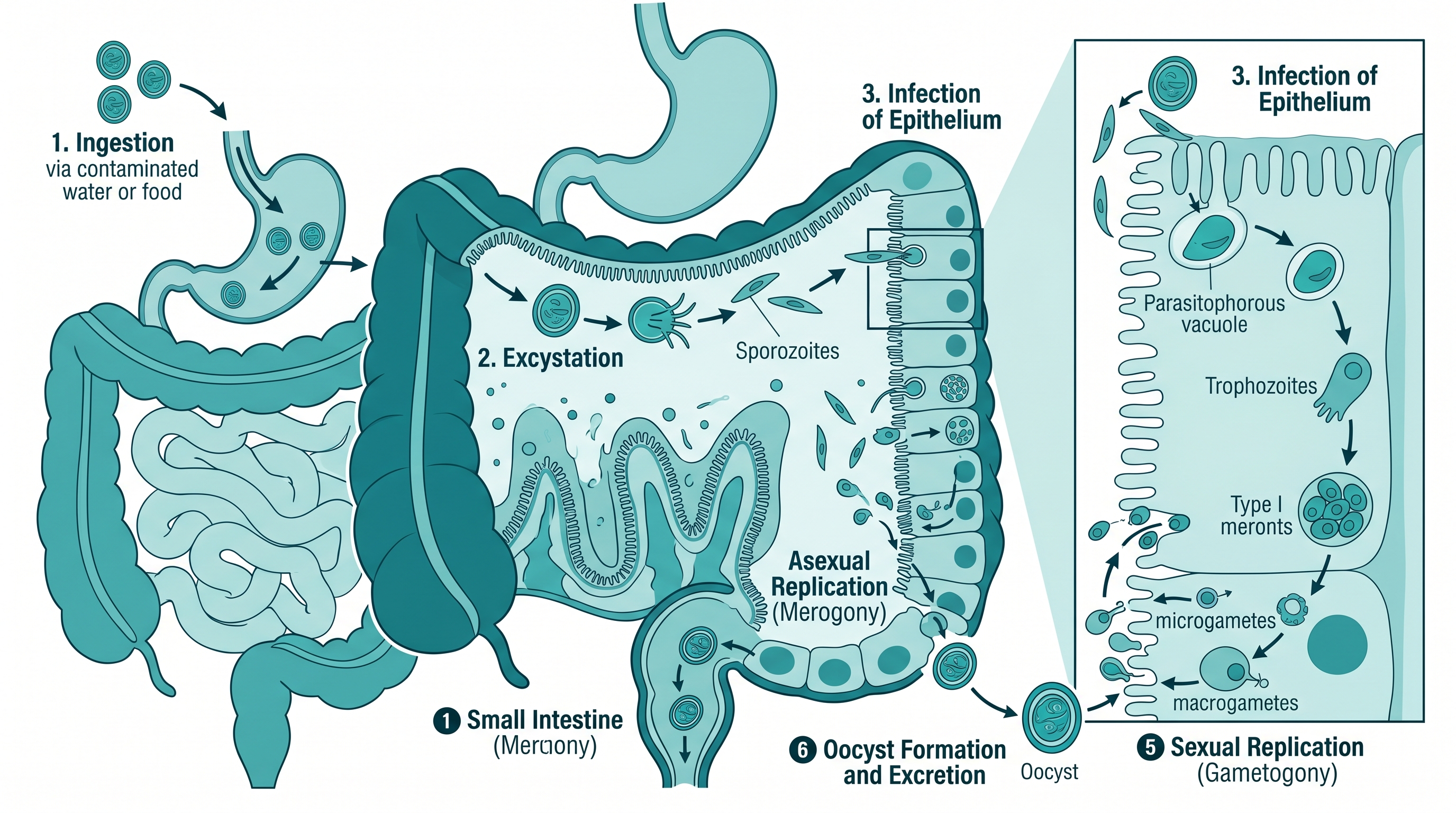
El ciclo completo se desarrolla dentro del mismo huésped:
- Se ingieren ooquistes con agua, alimentos o por contacto fecal-oral.
- En el intestino delgado, cada ooquiste libera cuatro esporozoítos que invaden las células epiteliales.
- Dentro de las células, el parásito pasa por varias generaciones asexuales (merogonia) produciendo merozoítos que infectan nuevas células.
- Finalmente se produce la fase sexual (gametogonia): se forman ooquistes de pared gruesa que salen con las heces y permanecen viables durante meses en el ambiente, y ooquistes de pared delgada que pueden reiniciar el ciclo dentro del mismo huésped (autoinfección).
Esta capacidad de autoinfección es importante: explica por qué en personas inmunodeprimidas la carga parasitaria puede crecer de forma incontrolable sin necesidad de nuevas exposiciones externas.
Formas de contagio de la criptosporidiosis
El agua: principal vía de transmisión
El agua contaminada es, con diferencia, la fuente más importante de infección. Y aquí viene el dato que más sorprende a la gente: los ooquistes de Cryptosporidium resisten el cloro a las concentraciones que se usan habitualmente para potabilizar el agua. El cloro, a dosis normales, simplemente no los mata.
Las únicas medidas de tratamiento del agua que eliminan eficazmente los ooquistes son:
- Filtración por membranas con poros de 1 micrómetro o menos.
- Tratamiento con luz UV — los ooquistes son especialmente sensibles a la radiación ultravioleta.
- Ebullición sostenida durante al menos un minuto.
- Ozono a dosis suficientes — más eficaz que el cloro, aunque menos habitual.
Los brotes asociados a agua de piscinas o parques acuáticos son especialmente frecuentes porque los nadadores pueden excretar ooquistes aunque ya no tengan síntomas, y el cloro no los elimina. Según los CDC, Cryptosporidium es la causa más común de brotes de enfermedad gastrointestinal relacionados con piscinas en Estados Unidos.
Transmisión persona a persona
La vía fecal-oral directa es la segunda en importancia. Con una dosis infectante muy baja — se estima que entre 10 y 100 ooquistes son suficientes para provocar infección — el parásito se transmite con facilidad en entornos de alta concentración como guarderías, residencias de mayores o cualquier lugar donde el control de higiene sea difícil de mantener.
Los niños en pañales son vectores eficientes: sus heces pueden contener millones de ooquistes, y el contacto con superficies contaminadas seguido de llevar las manos a la boca cierra el ciclo. Los padres, cuidadores y personal de guarderías son un grupo de riesgo secundario precisamente por esta razón.
Para entender mejor cómo detectar una infección parasitaria en general, la guía sobre cómo saber si tengo parásitos puede ser un buen punto de partida.
Contacto con animales
Como se mencionó antes, C. parvum tiene un reservorio animal importante, sobre todo en terneros y corderos jóvenes. El contacto directo con estos animales, manipulación de sus heces o incluso el agua de superficies agrícolas contaminada con sus deyecciones puede transmitir la infección. Los brotes rurales asociados a ferias de ganado o actividades de granja con niños están bien documentados en la literatura.
Grupos de riesgo
Personas con inmunodeficiencia
El grupo que más preocupa clínicamente son los pacientes inmunocomprometidos, especialmente aquellos con VIH/sida con recuento de linfocitos CD4 por debajo de 100 células/mm³. En este escenario, la criptosporidiosis deja de ser una gastroenteritis autolimitada y puede convertirse en una enfermedad crónica, diseminada y potencialmente mortal.
La infección puede afectar no solo al intestino delgado, sino extenderse al árbol biliar (colangiopatía por Cryptosporidium), a los pulmones y en casos excepcionales al páncreas. La diarrea crónica que resulta de estas formas graves puede provocar una desnutrición severa y una pérdida de peso que compromete aún más el pronóstico general del paciente.
Otros grupos de inmunodeficiencia con riesgo elevado incluyen los receptores de trasplantes de órganos sólidos bajo tratamiento inmunosupresor, los pacientes con deficiencias primarias de linfocitos T y quienes reciben quimioterapia mielotóxica.
Señal de alarma en pacientes con VIH
En personas con VIH y CD4 bajo, la diarrea acuosa persistente de más de 3 días, especialmente si se acompaña de pérdida de peso o ictericia, requiere evaluación urgente para descartar criptosporidiosis diseminada. El diagnóstico precoz y el tratamiento antirretroviral son determinantes en el pronóstico.
Niños pequeños y viajeros
Los niños menores de 5 años, especialmente los que asisten a guarderías o viven en zonas con saneamiento deficiente, tienen tasas de infección notablemente más altas que los adultos inmunocompetentes. En países de renta baja, la criptosporidiosis es una de las principales causas de diarrea infantil persistente y, junto con el rotavirus y el norovirus, uno de los responsables de desnutrición crónica en la infancia.
Los viajeros a países tropicales o en desarrollo conforman otro grupo de riesgo habitual. La llamada "diarrea del viajero" por Cryptosporidium tiene las mismas características que otros tipos — inicio brusco, diarrea acuosa — pero tiende a durar más que la causada por bacterias como E. coli enterotoxigénica.
Síntomas de la criptosporidiosis
Diarrea, calambres y el cuadro típico
El período de incubación oscila entre 2 y 10 días tras la ingestión de los ooquistes, con una media de unos 7 días. En personas inmunocompetentes, el cuadro es bastante homogéneo:
- Diarrea acuosa profusa: es el síntoma cardinal. Las deposiciones son muy líquidas, sin sangre, sin moco, y pueden llegar a 10-15 al día en los picos de la enfermedad.
- Calambres abdominales: dolor cólico, especialmente en la parte baja y media del abdomen, que suele ceder tras la deposición.
- Náuseas y vómitos: presentes en la mitad de los casos, especialmente al inicio.
- Fiebre leve a moderada: entre el 30% y el 50% de los pacientes presenta temperatura por encima de 38 °C, aunque rara vez supera los 39 °C en personas sanas.
- Fatiga y malestar general: cansancio notable que puede persistir más allá de la diarrea aguda.
- Pérdida de apetito.
En adultos sanos, el proceso es autolimitado y se resuelve en 1 a 3 semanas sin tratamiento. Sin embargo, la deshidratación puede ser significativa si la diarrea es intensa, y en niños pequeños puede requerir hidratación intravenosa. El patrón a veces es ondulante: los síntomas mejoran durante unos días y vuelven con fuerza antes de resolverse definitivamente.
Formas graves en inmunocomprometidos
En pacientes con inmunodepresión severa, la enfermedad adopta un carácter completamente diferente. La diarrea puede ser masiva — hasta 15-20 litros diarios en los casos más graves con VIH avanzado —, provocando una deshidratación y desequilibrio electrolítico que requiere manejo hospitalario intensivo. El adelgazamiento es rápido y pronunciado.
Cuando el parásito afecta las vías biliares, aparece dolor en el hipocondrio derecho, ictericia y elevación de enzimas hepáticas. Esta colangiopatía criptosporidiana es difícil de tratar y puede evolucionar hacia una insuficiencia hepática.
El riesgo de deshidratación
Aunque no es específico de la criptosporidiosis, la deshidratación es la complicación más inmediata a vigilar. Los signos que deben movilizar a buscar atención médica son: sed intensa y boca seca, disminución del volumen de orina y color oscuro de la misma, mareo al ponerse de pie, debilidad y confusión. En lactantes, la fontanela hundida y la ausencia de lágrimas al llorar son señales de alerta.
Diagnóstico de la criptosporidiosis
Tinción ácido-alcohol resistente
El diagnóstico de laboratorio es imprescindible porque los síntomas de la criptosporidiosis son prácticamente indistinguibles de los de otros protozoos como Giardia intestinalis o de gastroenteritis virales. El método clásico es la tinción de Ziehl-Neelsen modificada (o tinción ácido-alcohol resistente) aplicada sobre heces.
Los ooquistes de Cryptosporidium tienen la propiedad de retener la tinción fucsínica incluso tras el decolorante ácido — de ahí el nombre. Al microscopio, aparecen como estructuras rosadas o rojizas sobre un fondo verde-azulado si se usa la contratinción de malaquita. El tamaño de 4-6 micrómetros los diferencia de otros coccidios como Cyclospora (8-10 µm) o Cystoisospora (20-30 µm).
Un inconveniente: la excreción de ooquistes tampoco es constante, por lo que se recomienda analizar al menos dos o tres muestras recogidas en días distintos antes de descartar la infección.
Tests de antígenos (ELISA) y PCR
Igual que ocurre con otros parásitos intestinales, los métodos inmunológicos y moleculares han ganado terreno en el diagnóstico:
- ELISA de captura de antígenos: detecta proteínas del ooquiste en heces con una sensibilidad del 93-100% y especificidad similar. Es el estándar en muchos laboratorios de referencia, especialmente durante brotes, por su capacidad de procesar muchas muestras a la vez.
- Tests inmunocromatográficos rápidos: resultado en 15-30 minutos, útiles en urgencias o en entornos con recursos limitados. Sensibilidad algo inferior al ELISA pero muy práctica cuando hay urgencia diagnóstica.
- PCR (reacción en cadena de la polimerasa): la técnica más sensible disponible. Además de confirmar la infección con cargas muy bajas de parásito, permite identificar la especie (C. parvum vs. C. hominis) y el genotipo, información valiosa para estudios epidemiológicos y para guiar medidas de salud pública durante brotes. Su uso es principalmente hospitalario y de referencia.
Diagnóstico diferencial con otras parasitosis
Clínicamente, conviene distinguir la criptosporidiosis de otras infecciones protozoarias intestinales. La giardiasis produce síntomas parecidos pero con más gases y mayor tendencia a la cronicidad desde el inicio. La toxoplasmosis, aunque del mismo grupo coccidio, raramente produce síntomas intestinales en inmunocompetentes. Las amebiasis y shigelosis sí producen sangre en heces, lo que generalmente no ocurre en la criptosporidiosis. Un panel de diagnóstico multiplex por PCR puede resolver muchas ambigüedades clínicas en una sola determinación.
Tratamiento de la criptosporidiosis
Nitazoxanida en inmunocompetentes
En personas con un sistema inmune funcional, la criptosporidiosis se resuelve sola en la mayoría de los casos, pero el tratamiento farmacológico acorta la duración y la intensidad del cuadro. El único fármaco con evidencia de eficacia demostrada en ensayos controlados es la nitazoxanida.
La nitazoxanida actúa inhibiendo la piruvato:ferredoxina oxidorreductasa y otras enzimas del metabolismo anaerobio del parásito. La pauta estándar en adultos es 500 mg dos veces al día durante 3 días, con comida para mejorar la absorción. En niños, la dosis se ajusta al peso. Los estudios muestran una reducción significativa de la duración de la diarrea y de la excreción de ooquistes comparada con placebo.
En España y la mayor parte de Europa, la nitazoxanida no siempre está disponible en las farmacias habituales y puede requerir pedido especial. En Latinoamérica tiene mayor disponibilidad.
El problema en pacientes inmunocomprometidos
Aquí es donde la criptosporidiosis presenta uno de sus mayores desafíos clínicos: no existe un tratamiento farmacológico con eficacia demostrada de forma consistente en pacientes inmunodeprimidos graves. La nitazoxanida muestra resultados mucho más pobres cuando el sistema inmune no puede colaborar, y los estudios en pacientes con VIH avanzado no han demostrado curación microbiológica sostenida.
La estrategia más eficaz en estos pacientes es restaurar la función inmune:
- En pacientes con VIH, la terapia antirretroviral de gran actividad (TARGA) que eleva el recuento de CD4 por encima de 100 células/mm³ es, con diferencia, la medida más efectiva para controlar la infección. Muchos pacientes resuelven espontáneamente la criptosporidiosis cuando su sistema inmune se recupera bajo tratamiento antirretroviral.
- En trasplantados, reducir la inmunosupresión cuando sea posible puede contribuir al control.
El tratamiento de soporte — hidratación agresiva oral o intravenosa, control de electrolitos, nutrición parenteral si hay malabsorción grave — es fundamental en los casos severos.
Hidratación y cuidados de soporte
Independientemente del estado inmune, la hidratación es el pilar del tratamiento. Las soluciones de rehidratación oral (SRO) con la composición correcta de glucosa y sales son mucho más eficaces que el agua sola para compensar las pérdidas intestinales. En diarreas muy intensas o en pacientes que no toleran la vía oral, puede ser necesario el suero intravenoso.
Los antidiarreicos como la loperamida pueden aliviar los síntomas en adultos inmunocompetentes, pero deben usarse con precaución en niños y están contraindicados si hay fiebre alta o sospecha de infección bacteriana concomitante.
Prevención de la criptosporidiosis
Tratamiento del agua: lo que funciona y lo que no
Como se explicó antes, el cloro no es suficiente. Para agua destinada a bebida en contextos de riesgo:
- Ebullición: es la medida más simple y efectiva. Un minuto de ebullición (tres minutos a altitudes superiores a 2.000 metros) elimina los ooquistes con total seguridad.
- Filtros de membrana con poros ≤ 1 µm: retienen físicamente los ooquistes. Verificar que el filtro tiene certificación específica para protozoos, ya que no todos los filtros domésticos la tienen.
- Luz UV de baja presión: muy eficaz, especialmente en agua clara. Las lámparas UV portátiles son una opción razonable para viajeros.
- Cloración a dosis alta: concentraciones de cloro libre de 80 mg/L durante 30 minutos pueden reducir la viabilidad de los ooquistes, pero son incompatibles con el consumo normal y con las normas de calidad de agua potable.
Complementar con estrategias de desparasitación y prevención general puede ayudar a reducir el riesgo global de parasitosis intestinales.
Higiene de manos y prevención en entornos de riesgo
El lavado de manos con agua y jabón durante al menos 20 segundos es la medida de barrera más importante en la transmisión fecal-oral. El gel hidroalcohólico, tan habitual desde la pandemia de COVID-19, no elimina los ooquistes de Cryptosporidium — solo el jabón y el frote mecánico reducen la carga de forma significativa.
En entornos de alto riesgo (guarderías, hospitales, residencias):
- Cambio de pañales en zonas designadas, lejos de las áreas de preparación de alimentos.
- Lavado de superficies con solución de peróxido de hidrógeno al 3% o dióxido de cloro — el cloro doméstico a diluciones estándar es insuficiente.
- Exclusión de personas con diarrea activa de la preparación de alimentos o del cuidado de niños hasta al menos 48 horas después de la última deposición líquida.
Piscinas y espacios acuáticos
Dado que el cloro no inactiva los ooquistes, el control en piscinas públicas depende principalmente de la filtración y de prácticas de uso responsable. Las medidas recomendadas:
- No bañarse durante las 2 semanas siguientes a haber tenido diarrea por Cryptosporidium.
- No llevar al agua a niños con diarrea activa.
- Ducharse antes de entrar en la piscina.
- No tragar el agua de la piscina.
- Las piscinas con sistema de tratamiento UV son más seguras, pero no ofrecen garantía absoluta.
Recomendaciones para viajeros
Los viajeros a zonas con saneamiento deficiente deben seguir las precauciones habituales para la diarrea del viajero, pero con especial atención a las vías que el cloro no cubre. La regla general: solo agua embotellada de sello intacto o agua hervida para beber, incluyendo los cubitos de hielo y el lavado de dientes. Evitar frutas peladas por terceros, ensaladas en establecimientos de baja confianza y mariscos crudos.
Criptosporidiosis vs. otras parasitosis intestinales
Situar la criptosporidiosis en el contexto de otras infecciones parasitarias ayuda a entender sus peculiaridades:
- vs. Giardia: ambas se transmiten por agua y producen diarrea acuosa, pero Giardia suele dar más gases y distensión. La giardiasis responde bien al metronidazol; la criptosporidiosis, no. Ambas resisten el cloro convencional.
- vs. Amebiasis: la amebiasis produce sangre en heces (disentería) lo que no ocurre habitualmente en la criptosporidiosis. Además, la amebiasis puede diseminarse al hígado formando abscesos.
- vs. Toxoplasmosis: el Toxoplasma raramente produce síntomas intestinales en inmunocompetentes, mientras que la criptosporidiosis siempre afecta al tracto digestivo. En inmunodeprimidos, ambos son parásitos oportunistas graves. Más información en el artículo sobre toxoplasmosis síntomas y contagio.
- vs. Enterobius (oxiuros): los oxiuros producen picor anal nocturno, no diarrea. Son helmintos visibles a simple vista, mientras que Cryptosporidium es microscópico.
Para comparar con otras parasitosis frecuentes, el artículo sobre Giardia intestinalis síntomas y tratamiento ofrece un análisis similar con otra de las principales causas de diarrea parasitaria.
Preguntas frecuentes sobre criptosporidiosis
¿La criptosporidiosis se cura sola en personas sanas?
En adultos y niños mayores con el sistema inmune intacto, sí. La infección es autolimitada y se resuelve en 1 a 3 semanas. La nitazoxanida puede acortar ese tiempo, pero no es imprescindible en casos leves. La prioridad es mantener una buena hidratación para compensar las pérdidas por diarrea y prevenir complicaciones.
¿Por qué el cloro no elimina el Cryptosporidium?
Los ooquistes tienen una cubierta proteica muy resistente que los protege de los oxidantes habituales. El cloro libre a 1-3 mg/L, que es la concentración habitual en redes de agua potable, no inactiva los ooquistes viables. Solo el calor sostenido, los filtros de membrana de menos de 1 micrómetro y la radiación UV a dosis suficientes destruyen de forma fiable los ooquistes.
¿Cuánto tiempo puede estar el parásito en el ambiente?
Los ooquistes son notablemente resistentes en condiciones ambientales favorables. En agua fría y con poca materia orgánica pueden permanecer viables durante varios meses. En suelo húmedo, también semanas o meses. La desecación y las temperaturas extremas (por encima de 60 °C o por debajo de −20 °C de forma sostenida) los inactivan. En superficies secas a temperatura ambiente, la viabilidad cae en días.
¿Se puede contagiar de un animal de compañía?
El riesgo existe pero es relativamente bajo. Los perros y gatos pueden albergar Cryptosporidium, pero los genotipos que más frecuentemente los afectan no son los mismos que infectan a humanos. Con buena higiene de manos tras manejar heces de animales y evitar el contacto directo durante la fase de diarrea del animal, el riesgo es mínimo para personas sanas. En inmunocomprometidos, la precaución debe ser mayor.
¿Qué diferencia hay entre criptosporidiosis y criptococosis?
Son infecciones completamente distintas causadas por microorganismos sin relación. La criptosporidiosis está causada por el protozoo Cryptosporidium y afecta principalmente al intestino. La criptococosis está causada por el hongo Cryptococcus neoformans y afecta principalmente al sistema nervioso central en pacientes inmunodeprimidos. La similitud fonética del nombre genera confusión, pero son enfermedades diferentes con diagnóstico y tratamiento distintos.
¿Es peligrosa la criptosporidiosis durante el embarazo?
En mujeres embarazadas inmunocompetentes, la criptosporidiosis sigue siendo autolimitada, pero el riesgo de deshidratación es mayor y debe gestionarse con más cuidado. No hay evidencia sólida de que el parásito cruce la placenta ni de que aumente el riesgo de malformaciones. La nitazoxanida no tiene datos de seguridad suficientes en embarazo y suele evitarse, especialmente en el primer trimestre. El manejo es principalmente de soporte.
Conclusión
La criptosporidiosis es un ejemplo de cómo un parásito microscópico puede plantear desafíos importantes a la salud pública precisamente por sus características biológicas: resistencia al cloro, dosis infectante baja, alta excreción de formas infectantes y comportamiento muy diferente según el estado inmunológico del huésped.
En personas sanas, el problema es molesto pero manejable con hidratación y, si se decide tratar, con nitazoxanida. En personas inmunodeprimidas, especialmente con VIH avanzado, la clave está en restaurar la función inmune más que en buscar un antiparasitario eficaz, porque hoy no existe ninguno con eficacia demostrada de forma consistente en ese contexto.
La prevención sigue siendo la herramienta más poderosa: entender que el cloro no es suficiente, que la ebullición y la filtración sí funcionan, y que el lavado de manos con agua y jabón es irremplazable. Para seguir aprendiendo sobre parasitosis intestinales, consulta nuestra guía sobre síntomas y tratamiento de parásitos intestinales o el artículo sobre desparasitación natural.